
A Química estudia, fundamentalmente, as transformacións dunhas substancias en outras para obter determinados productos ou para evitar a súa formación. Este estudio esixe o coñecemento das leis que rexen os cambios químicos, as cales dependen da estructura dos materiais. Para comezar, lembrarémonos do modelo cinético da materia:

e despois clasificarémolos segundo o esquema:
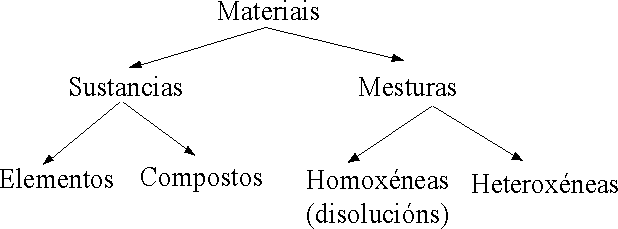
A materia está formada basicamente por elementos e compostos, que se poden presentar como substancias puras ou como mesturas. Un composto é unha substancia con dous ou máis elementos combinados quimicamente. Un elemento é único. Cada composto ten as súas propiedades características (densidade, conductividade, solubilidade, etc), as cales serven para distinguilo experimentalmente dos demais e para separalo das mesturas.
Leis empíricas das combinación químicas
Son o conxunto das primeiras leis experimentais descubertas ao medir os pesos e os volumes dos elementos que reaccionan para formar compostos.
1.- Lei de Conservación da masa (Lavoisier): nun sistema pechado (que non intercambia materia co exterior) a masa total dos reactivos debe ser igual á dos productos.
2.- Lei das proporcións constantes (Proust): cando dous ou máis elementos se unen para formar un mesmo composto, a proporción de combinación en peso é sempre a mesma.
Dalton interesouse pola elaboración dunha teoría atómica da materia para explicar teoricamente as leis experimentais anteriores. Propuxo (1808) as seguintes hipóteses:
Os átomos, por razóns dimensionais obvias, non se poden ver, pesar, etc. individualmente. Sen embargo, si que é posible determinar a súa masa relativa (masa atómica) respecto aos outros elementos empregando a lei das proporcións definidas e o punto 2. da teoría de Dalton. Se ademais coñecemos a fórmula e as masas atómicas dos elementos é doado calcular a masa molecular sumando as masas dos átomos que forman a sustancia
Nota: Observa que a masa atómica relativa depende de que a fórmula estea correctamente escrita.
Para determinar a fórmula dunha substancia Dalton propuxo unha regra de máxima simplicidade: cando dous elementos se poden combinar dunha única meneira, a combinación é binaria (AB), pero se hai outras combinacións a máis estable é a binaria (AB) e as outras ternaria (A2B, AB2), etc. As fórmulas obtidas dependen da corrección da hipótese binaria.
Despois de todo, aínda non había resposta segura á pregunta .. ¿canto pesa un átomo?. A solución veu, sorprendentemente, do estudio das leis dos gases polas razóns que veremos de contado.
3.-Lei dos volumes de combinación (Gay-Lussac):Os volumes, medidos nas mesmas condicións de P e T, das substancias gaseosas que participan nunha reacción química están en relación de números enteiros sinxelos.
4.- Principio de Avogadro:Se as condicións físicas (P,T) son as mesmas, un mesmo volume de calquera gas contén o mesmo número de moléculas. Cando Avogadro enunciou esta lei tivo que modificar o concepto de ''átomo composto'' de Dalton e propoñer un novo de molécula. Unha molécula está formada pola unión de dous ou máis átomos simples (pero non é unha partícula unitaria atómica, como pensaba Dalton). As moléculas dos elementos simples (hidróxeno, osíxeno, nitróxeno ..) son diatómicas (hipótese) e o seu tamaño é moito menor (practicamente despreciable) que a distancia entre elas.
*nota: Esta hipótese explica a lei de Gay-Lussac, porque o volume que ocupa un gas (segundo Avogadro) non depende do tamaño das moléculas senón das distancias entre elas, e estas son moito máis grandes que o tamaño molecular. Pódese comprobar que esta lei tamén proporciona un método para comparar os pesos das moléculas: se collemos volumes iguais de diferentes gases nas mesmas condicións de P e T e despois pésamolos e comparámolos, podemos relacionar as súas masas moleculares relativas, porque o número de moléculas que hai é o mesmo (d1/d2 = MM1/MM2).Concepto demol
Por razóns que xa vimos antes non podemos dispoñer dos átomos individualmente, o cal fai necesario definir unha unidade cómoda para traballar con eles. Os químicos inventaron un número útil, chamado número de Avogadro2 ou mol, NA = 6,023×1023 unidades. Definimos o mol como o número de Avogadro de individualidades (átomos, moléculas, ións, electróns, etc.). ¿Por que é práctico este número? .. porque se escolleu de forma tal que un mol de individualidades atómicas ou moleculares pesa o mesmo que a masa atómica ou molecular expresada en gramos.
P.ex: un mol de átomos de Fe (MAt = 55,85 / u) pesa 55,85 / g. Un mol de moléculas de auga (Mmolec=18 / u) pesa 18 / g, etc.
Vemos que é doado pasar de gramos a moles e viceversa pola relación sinxela:
As reaccións químicas prodúcense preferentemente en fase gas ou en disolución, polo que a continuación comentaremos algunhas propiedades destes medios:
As disolucións son mesturas homexéneas de dous ou máis compoñentes. Poden ser gaseosas, líquidas ou sólidas.
As primeiras obtémolas cando mesturamos gases, como todos os gases mestúranse en calquera proporción, todas as mesturas de gases son homoxéneas e polo tanto disolucións.
As disolucións líquidas fórmanse cando disolvemos nun líquido unha substancia en calquera dos seus estados: sólido, líquido ou gas. Se o disolvente é auga, a disolución chámase acuosa. Cineticamente as moléculas de soluto (a substancia que se disolve e está en menor proporción) atópanse distribuídas homoxeneamente en todo o volume da disolución.
Nas disolucións sólidas un dos compoñentes está disperso dentro do outro que se atopa en estado sólido. As máis importantes son as aliaxes.
Nas substancias ou compostos químicos as proporcións que interveñen na combinación son fixas e determinan a fórmula da substancia. Como nas disolucións a proporción de mestura é variable, non hai "fórmula" para unha disolución, entón as propiedades dependen dunha magnitude chamada concentración, que mide a proporción de mestura entre o soluto e o disolvente.
A concentración dunha disolución exprésase normalmente dalgunha das seguintes maneiras:A) gramos por litro(C): representa os gramos de soluto por litro de disolución:
C = gS/VD(lit)
B) molaridade (M): representa os moles de soluto por litro de disoluciónM =nS/VD(lit)
C)porcentaxe de soluto(%):
C.1) en masa: representa os gramos de soluto por cada 100 g de disolución:
% masa = (mS/mD)×100
C.2) en volume: representa o volume de soluto por cada 100 das mesmas unidades de volume de disolución:
% vol = (VS/VD)×100
Símbolos: s -> soluto d -> disolvente D -> disolución
O estado gasoso é o máis fácil de estudiar porque as interaccións entre as súas moléculas son practicamente despreciables en condicións normais:
-> Segundo a lei de Boyle, se comprimimos isotermicamente (a T = Cte) un gas e comparamos a presión e o volume antes e despois da compresión, cúmprese que P1V1 = P2V2 ; ou PV = K'
-> Segundo a lei de Gay-Lussac, se enfriamos a P = Cte un gas e comparamos os volumes e as temperaturas (expresadas en K) iniciais e finais, V1/T1 = V2/T2; e en xeral: V/T=K"
Destas leis pódese deducir PV/T = r (Lei dos gases ideais), onde r é unha constante a determinar experimentalmente para cada mostra particular de gas. Sen embargo, tendo en conta o Principio de Avogadro -o volume que ocupa un gas é proporcional ao número de moléculas (ou moles) que hai contidas no recipiente, V = Kn- e chamando ao producto KK'K" = R, obteremos a Ecuación de estado dos gases ideais:
Esta ecuación podémola aplicar tamén ao caso dunha mestura de gases (disolucións gasosas).
Composición centesimal e fórmula
Saber a fórmula dun composto é moi importante por que dá o número e os átomos presentes na substancia. Podemos empregala para determinar a porcentaxe en masa dos elementos que interveñen, p.ex. para AXBY, %masaA = (MatA×X/Mmolec)×100, e a relación molar (ou individual) entre os elementos. Sen embargo é máis interesante determinar a fórmula a partir do coñecemento -mediante experimentos- da %masa. O procedemento consiste sinxelamente en calcular os moles de cada elemento e determinar con eses moles a proporción molar de combinación máis sinxela (dividindo polo menor) -fórmula empírica-. Coa fórmula empírica e o peso molecular da substancia (determinado aplicando outras leis físico-químicas), podemos determinar a fórmula exacta porque é un múltiplo enteiro da empírica.
No capítulo anterior vimos que as substancias teñen unha fórmula única que informa da proporción de combinación atómica e másica entre os elementis, p.ex. a auga é H2O, o amoníaco NH3, etc., sen embargo aínda non sabemos por que a proporción de combinación é esa precisamente e non outra calquera como p.ex. N2H3 ou NH4, etc... a resposta intuimos que debe estar na propia estructura dos átomos.
O experimento de Rutherford, que vimos no curso anterior, propón un modelo de átomo formado por un núcleo central que contén case toda a masa e a carga positiva (protóns e neutróns) e unha cortiza onde están as cargas negativas (electróns), así que definimos os seguintes conceptos:
Número atómico (Z): o número de protóns que ten un átomo no núcleo. Como todos os átomos son electricamente neutros, no estado fundamental o número atómico debe ser igual ao número de electróns da cortiza.
Elemento químico: o conxunto de todos os átomos que teñen o mesmo Z.
Número másico (A): representa a masa dun átomo e calcúlase sumando o número atómico (Z) e o número de neutróns (N), entón A = Z + N.
Non todos os átomos do mesmo elemento teñen o mesmo A, porque o número de neutróns e outras partículas do núcleo pode non coincidir. Ao conxunto de átomos dun mesmo elemento onde se dan estas circunstancias chámaselles ISÓTOPOS. Dous isótopos dun mesmo elemento distínguense porque teñen o número de masa diferente, pero o seu número atómico é o mesmo.
Maso atómica: o promedio das masas dos isótopos dun elemento.
Modelo de Bohr
Bohr intentou aplicar as ideas precuánticas de Planck-Einstein ao átomo de Rutherford para adaptalo aos novos resultados experimentais (espectros de gases incandescentes). As súas ideas sobre o comportamento dos electróns no interior do átomo podémolas resumir así:
Os elementos descubríronse lentamente e con moitas dificultades. Despois do cal fíxose necesaria a súa clasificación sistemática cun criterio científico. A principios do século XIX os químicos observaron que moitos deles podían agruparse en familias con propiedades químicas semellantes. No 1869 o químico ruso Mendeleieff obtivo éxitos importantes: ordenou os elementos coñecidos segundo os pesos atómicos crecentes por periodos e despois escribiu verticalmente os de propiedades semellantes, de forma parecida ao modelo actual. Os elementos semellantes no comportamento químico pertencían á mesma columna, ou familia. Aos elementos descoñecidos correspondíalles un espacio baleiro na táboa periódica, pero podíanse predicir as súas propiedades máis importantes coñecendo a columna e o período onde debería estar situado (promediando os valores das propiedades dos elementos veciños). Cando se descubrían e as propiedades coincidían coas previstas o feito representaba un gran éxito para o novo criterio de clasificación.
Cando no século XX se profundizou na estructura dos átomos e se descubriu o concepto de número atómico, os científicos comprenderon inmediatamente que este número representa o criterio óptimo para clasificar os elementos: é un número enteiro que varia regularmente dun elemento ao seguinte e o peso átomico non.
No Sistema Periódico actual os elementos están ordenados en sete filas horizontais ou períodos. O primeiro período contén dous elementos e chámase "moi curto", os dous seguintes teñen oito elementos cada un e chámanse periodos "curtos". Os períodos catro e cinco "longos" e teñen 18 elementos. Por último os sexto e séptimo son os "moi longos" e teñen 32 elementos. Máis importante que a ordenación horizontal é a vertical, porque nas columnas sitúanse os elementos da mesma familia química. O SP ten dúas series: "A" ou serie principal e "B" ou serie de transición.
Podemos concluír dicindo que os elementos coas propiedades parecidas teñen o mesmo número de electróns na súa última capa. Estes electróns chámanse "electróns de valencia" e os outros "electróns internos". As propiedades químicas dun elemento dependen do número de electróns de valencia. Ímonos fixar no grupo VIII (gases nobres). Agás o primeiro, Helio, que ten a última capa completa (con 2 e-), os outros teñen oito electróns na última capa. O feito de que estes elementos non reaccionen químicamente (ou moi pouco) suxire que esta estructura (8 e( na capa de valencia) é unha estructura quimicamente moi "estable". Todos os outros elementos son quimicamente "inestables". Esto quere dicir que se combinan uns cos outros para acadar estructura electrónica de gas nobre, en concreto do gas nobre que teñen máis perto... ¿como é posible?, gañando, perdendo ou compartindo electróns, é dicir, mediante combinación química cos outros elementos (mediante enlaces químicos), pero... ¿cales elementos gañan, perden ou comparten os electróns?, en ¿que combinacións?. Para responder a esta importante pregunta definiremos previamente o concepto de Enerxía de Ionización.
A Enerxía de Ionización é a enerxía absorbida no proceso de separación do último electrón dun átomo: A(g) + Ei → A+(g) + 1e-
Segundo esta definición, se Ei é pequena quere dicir que non é difícil quitarlle un electrón ao átomo. Os elementos do Sistema Periódico que teñen Ei↓ non atraen con moita forza aos electróns da capa de valencia. Contrariamente, os que teñen Ei↑ atraen fortemente aos electróns da última capa. Entre estes dous estremos hai elementos que posúen Ei intermedias. Esta conclusión permite clasificar aos elementos nos seguintes grupos:
metais: Son os elementos con Ei↓. Perden "facilmente" os electróns da capa de valencia. Forman, preferentemente, ións positivos.
non-metais: Són os elements coas Ei↑. Non perden facilmente os electróns. Normalmente cóllenos. Forman preferentemente ións negativos.
semi-metais: compórtanse como metais cos non-metais e como non-metais cos metais. Teñen propiedades intermedias.
gases nobres: Os que normalmente non forman ións.
O Sistema Periódico está dividido por unha liña quebrada: á esquerda da cal están os metais e á dereita os non-metais, os semi-metais son os elementos que se sitúan na beira da liña e na columna VIII os gases nobres.
O hidróxeno aínda que se sitúa na primeira columna non é un metal, é un non-metal ao que lle corresponde unha posición química entre o carbono e o nitróxeno.
Respecto ao número de electróns perdidos ou gañados cumpre dicir que perder ou gañar máis de tres electróns é imposible.
Cando os átomos están situados a distancias curtas interactúan entre eles. Chamaremos enlace químico á interacción que se produce entre dous ou máis átomos, cando o resultado é a formación dun composto estable. Calquera teoría do enlace químico debe explicar por que hai átomos que se unen e outros non. Todas as teorías propostas intentan xustificar a relación entre enlace químico, estructura da materia e as propiedades físicas e químicas.
Para describir o enlace químico imos utilizar o modelo e símbolos de Lewis-Kossel:
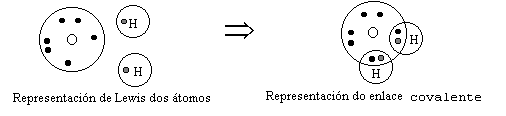
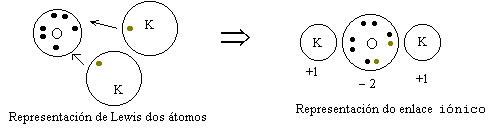
No proceso de formación dun enlace sempre hai cambios de enerxía. Para separar os átomos que forman un composto hai que romper o enlace. Isto acádase dando ao conxunto unha enerxía igual ou un pouco maior da que se desprende cando se forma o enlace. Esta enerxía chámase enerxía de enlace. A enerxía de enlace é unha medida da estabilidade do enlace. Canto máis grande sexa máis estable será o enlace. Significa que hai que aportar máis enerxía para romper a unión. Os enlaces químicos explican as propiedades das substancias.
Enlace iónico
Prodúcese cando hai unha transferencia de electróns entre un átomo metálico (con Ei↓) e outro non metálico (con Ei↑), convírtense en ion positivo e negativo respectivamente. A forza que mantén unidos aos ions é de tipo eléctrostático entre cargas eléctricas de signo contrario. Na maioría dos casos o número de electróns gañados e perdidos e tal que os ions resultantes teñen configuración electrónica de gas nobre (8 e- na última capa). As substancias iónicas non están formadas por parellas de ións ou por pequenas agrupacións. Cada un dos ions ten tendencia a situarse entre ions con carga eléctrica oposta á súa, formando unha rede sólida cristalina cunha gran cantidade de ións positivos e negativos ordenados alternativamente. A fórmula dunha substancia iónica é o conxunto máis pequeno de ións que resulta electricamente neutro. Exemplos: CaF2, KBr, Al2O3, MgO, etc.
Enlace covalente
Cando os átomos teñen a mesma Ei (e grande), é dicir, a mesma atracción polos electróns da capa máis externa, non se pode producir unha transferencia electrónica entre os átomos. Polo que non se vai a formar un cristal iónico. Fórmase unha molécula na que os átomos mantéñense unidos por enlaces covalentes onde se comparten as parellas de electróns. Son exemplos deste tipo de substancias: O2, F2, N2, ICl, H2O, NH3, NF3, SO. Sen embargo, tamén hai casos en que se forman sólidos pola unión de átomos mediante enlaces covalentes, localizados entre os átomos e distribuidos tridimensionalmente nunha "molécula xegante". Estas substancias chámanse sólidos con redes tridimensionais. P.ex: Diamante (C), Carburo de Silicio (SiC), etc.
Enlace metálico
Como os metais (Ei↓) teñen poucos electróns na capa de valencia non poden formar moléculas individuais, non dispoñen de suficientes electróns na capa de valencia para que a molécula cumpra a regra dos oito electróns. P.ex., o sodio ten 1 e- na última capa e dificilmente podería cumprir a regra compartindo 8 electróns. Tampouco é posible a formación de ions positivos e negativos, porque ao seren os átomos dun mesmo elemento químico, non se pode imaxinar que un perda electróns e o outro gañe. O modelo que explica o enlace entre os átomos metálicos, consiste na formación dunha rede cristalina de catións metálicos unidos por electróns compartidos nun orbital de enlace de toda a rede. Exemplos: metais (Fe, Al, Na, Cu) e aliaxes.
Forzas intermoleculares
As sustancias moleculares poden atoparse en diferentes fases (sólido, líquido ou gas). As forzas de cohesión son as responsables da interacción entre as súas moléculas,m estan forzas poden clasificarse en: forzas de London (prodúcense sempre entre moléculas apolares ou polares), forzas dipolares (entre moléculas polares) e por último tamén é importante a forza de enlace por ponte de hidróxeno (entre H e un elemento con Ei moi grande e tamaño pequeño: F, O, N).
1O concepto de átomo composto de Dalton NON é o mesmo que o de molécula formada pola unión de átomos. Dalton pensaba que un átomo composto era unha partícula.
2É o número de átomos que hai en 0,012 / kg de 12C -patrón de referencia-.