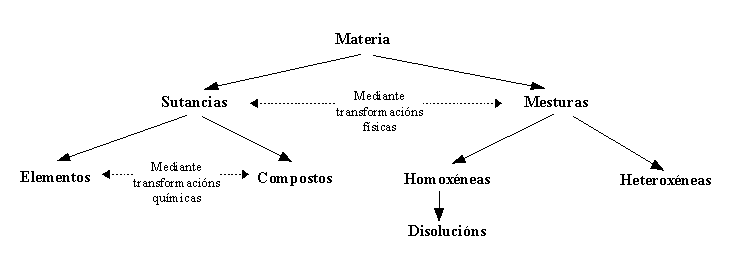
Os materiais, para o seu estudio, podemos clasificalos así:

As leis ponderais son experimentais, J. Dalton intentou explicalas mediante unha teoría que propón un modelo de materia que caracteriza as substancias nun nivel atómico-molecular e un concepto de cambio químico como redistribución de átomos, que explican as leis cuantitativas experimentais comprobadas. Dalton edificou a súa teoría enunciando varias hipóteses que podemos resumir así:
Cando Dalton establece que os átomos dun mesmo elemento son iguais entre si e diferentes aos dos outros elementos está a introducir o concepto de masa atómica. Chegou a afirmar que a diferencia entre os átomos estaba precisamente na masa atómica, en contra das ideas da época, segundo as cales eran outras propiedades como a forma, color, tamaño, etc.
A lei das proporcións definidas e a teoría de Dalton permiten a posibilidade de calcular as masas dos átomos (se escollemos un deles como patrón); sen embargo, é necesario coñecer a fórmula concreta dos compostos. Este feito obrigou a Dalton a emitir outra hipótese, chamada hipótese de máxima simplicidade: a fórmula dos compostos binarios máis probable é a que corresponde á relación máis sinxela entre o número de átomos que forman a molécula, é dicir 1:1. P.ex. segundo Dalton a fórmula da auga era HO.
Podemos comentar algunhas experiencias que obrigaron a modificar algunhas das ideas de Dalton, especialmente o seu modelo de gas e a hipótese de máxima simplicidade.
Gay-Lussac estudiou as relacións volumétricas que se daban nas reaccións químicas entre gases e alcanzou uns resultados que non se podían xustificar coa teoría de Dalton. A relación volumétrica de Gay-Lussac na reacción entre o osíxeno e o hidróxeno para formar auga foi: 1 volume de osíxeno e 2 volumes de hidróxeno, nas mesmas condicións de P e T, reaccionaron para formar exactamente 2 volumes de auga. Estes resultados amosan contradiccións coa teoría.
O modelo de gases de Dalton (modelo continuo) está en contradicción cos resultados. Pero se supoñemos que as partículas son moléculas di, tri, etc.-atómicas, e queo tamaño das moléculas non inflúe no volume que ocupa o gas -hipótese de Avogadro- os resultados son lóxicos.
A ordenación dos elementos. O sistema periódico
BOYLE, no ano 1661, definía aos elementos como as susbtancias químicas que non se poden separar en diferentes compoñentes por ningún medio, o cal quere dicir que hai tantas clases de átomos como elementos.
Cando no século XIX o número de elementos coñecidos fíxose cada vez maior xurdiu a necesidade de clasificalos sistematicamente en grupos con propiedades químicas semellantes - familias-. P.ex: os elementos da columna II: forman os mesmos óxidos (XO), os mesmos hidróxidos X(OH)2, etc., e as súas propiedades físicas varían regularmente cando baixamos ou subimos na columna.
Sen embargo isto non é todo,.. citando a Mendeleiev ''para unha verdadeira comprensión da materia é moi importante notar que todos os aspectos da distribución dos elementos, de acordo cos seus pesos atómicos, expresa, esencialmente, unha única dependencia fundamental - as propiedades periódicas-''. Isto significa que, ademais da variación regular nas propiedades físicas e químicas, dentro de cada familia, tamén hai un cambio periódico desas propiedades entre os elementos dunha liña horizontal (período), é dicir as propiedades dos elementos, igual que as formas e propiedades dos seus compostos son función periódica dos pesos atómicos (actualmente sabemos que é dos números atómicos)dos elementos -lei periódica-.
No curso de 3-eso vimos que as partículas das sustancias (as moléculas) estaban formadas pola unión (enlace) de átomos e para comprender as propopiedades fisico-químicas das sustancias necesitamos saber como están unidas (enlazadas) as súas partículas. Isto só podemos comprendelo se temos un MODELO ATÓMICO que explique como é posible -mediante que mecanismo- se poden enlazar os átomos.
O curso anterior estudiamos un modelo -proposto por J. Thomson a principio do século XX- baseado nas forzas eléctricas que explicaba a conductividade eléctrica dos materiais. Iste modelo dicia que ''os átomos son unha especie de esferiñas dun tamaño aproximado de 10-10 m onde os electróns (as cargas eléctricas negativas) están localizados no interior dunha distribución continua de carga positiva''. O modelo de Thomson estivo vixente durante pouco tempo, pois un científico ''defensor convencido'' do modelo (E. Rutherford) tentou comprobar se o modelo era EXPERIMENTALMENTE correcto. Para comprobalo ideou un experimento que foi ''crucial'' para entender a constitución interna do átomo
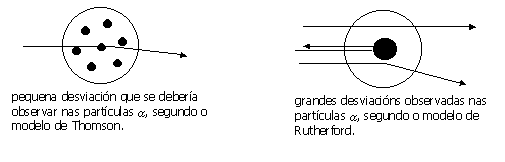
Os resultados do experimento amosaron unha ''estrutura sorprendente'': Hai un núcleo central co 99,9% da masa e toda a carga positiva, o seu diametro (tamaño) é 0,0001 veces máis pequeno que o do átomo. As cargas negativas (electróns) deben estar na cortiza ao redor do núcleo. A maior parte ddo átomo está baleiro (non hai nada) e se as cargas positivas están concentradas no núcleo ... por que non estoupa??, a masa das cargas positivas e negativas é a masa do átomo??, como se atopan as cargas negativas no interior do átomo??, se están no exterior por que non caen sobre o núcleo se son atraidas por iste??
Algúns experimentos posteriores permitiron responder a estas importantes cuestións ... :
primeiro, a masa do átomo non é a suma das masas dos protóns (cargas positivas) e dos electróns (cargas negativas, de masa moi pequena 0.005 veces a do protón), e polo tanto debería haber unha terceira clase de partículas (con carga eléctrica 0 e masa similar á do protón) para que a masa medida experimentalmente cadrase coa prevista teoricamente. Por outra banda se o núcleo non estoupa é porque debe haber FORZAS NUCLEARES de unión entre as partículas do núcleo máis intensas cas eléctricas e de curto alcance -do orden do tamaño do núcleo-. Fóra do núcleo estas forzas non mse manifestan, non se notan. Logo, temos un NÚCLEO formado por particulas positivas (protóns) e particulas sen carga (neutróns) que exercen entre si forzas nucleares atractivas e forzas eléctricas repulsivas -son máis intensas as forzas nucleares cas eléctricas- e a masa (chamada número de masa, A) do átomo é a suma das masas dos protóns (Z) e dos neutróns (N), polo que A = Z + N. Todos os átomos dun mesmo elemento teñen igual Z, sen embargo N pode ser diferente e en consecuencia A tamén -isótopos-. A masa dun átomo é a media ponderada da masa dos seus isótopos.
**NOTA: a existencia dos isótopos fai recomendable escoller como patrón de unidades de masas atómicas a escala baseada no isótopo 12C, de xeito que este isótopo ten unha masa atómica 12,0000 / u (exacta).
segundo, os electróns deben estar xirando na CORTIZA cunha velocidade suficientemente grande para ''non caer'' sobre o núcleo, se estivesen en repouso caerían inmediatamente -pola atracción eléctrica núcleo e electrón- colapsando o átomo -o cal non acontece porque sabemos que a materia é relativamente estable-, e o movemento debe ser semellante ao dos satélites que orbitan ao redor dos planetas. Estudios e experimentos posteriores tamén amosaron que os electróns non se atopan xuntos orbitando ao redor do núcleo, senón que estan ordenados en CAPAS (ou NIVEIS de enerxía) e en cada capa hai un límite máximo de electróns que collen nela. Desde o punto de vista da química a parte máis importante do átomo é a cortiza -particularmente a capa máis externa da cortiza- porque é á que podemos chegar máis facilmente -a máis accesible- mediante unha combinación química entre dous átomos.
Para que dous (ou máis) átomos resulten enlazados deben colisionar entre si -lembremos o modelo de reacción química estudiado no curso anterior- e como consecuencia deben resultar afectados os átomos -particularmente a capa máis externa-.
Como consecuencia da colisón son posibles dous mecanismos básicos de enlace: a) cando hai unha TRANSFERENCIA de electróns dun átomo a outro -formando ións positivos e negativos respectivamente, enlace iónico- onde a forza de unión entre os ións resultantes será de atracción eléctrica e b) cando os átomos resultan enlazadas pola COMPARTICIÓN de electróns, onde a unión tamén é de tipo eléctrico pero de forma diferente á anterior -enlace covalente-.
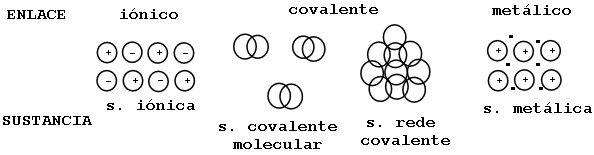
Estes dous mecanismo explican a diversidade de sustancias que coñecemos?? fundamentalmente si, pero con variacións. O máis importante é entender como afectan estes tipos de enlace ás propiedades das sustancias. Hai tres tipos de enlace químico (iónico, covalente, metálico) e catro tipos de sustancias: iónicas, moleculares covalentes, redes sólidas covalentes e metálicas. As propiedades físico-químicas -Conductividade, Solubilidade, Punto de fusión, etc.- destas sustancias poden deducirse e comprenderse se coñecemos o tipo de unión entre as súas partículas.
Tamén é importante ver que agora podemos predicir que propiedades terá unha sustancia se sabemos como están unidas as súas partículas, é dicir ... se o átomo A enlaza co átomo B que tipo de composto formarán?? A resposta é obvia: depende de que ''clase de átomos'' sexan A e B. En principio, hai dúas clases de átomos no SP: os metais que forman sen moita dificultade ións positivos e non-metais (perden e-) que forman facilmente ións negativos (gañan e-) e suporemos que os gases nobres non reaccionan. Entón:
Segundo vimos o curso anterior unha reacción química é unha transformación entre susbtancias que se produce como consecuencia de choques entre moléculas, reordenándose os átomos de forma diferente á inicial. Segundo este modelo os átomos permanecen inalterados, non cambian durante a transformación.
Se o número de átomos é igual ao principio e ao final e estes non cambian (todos os átomos da mesma substancia teñen a mesma masa) é doado deducir que en todas as reaccións a masa debe conservarse -Lei de conservación da masa-
mreac = mprod
Outra lei básica na interpretación da química é a que fai referencia á relación entre as masas dos elementos que forman un composto AxBy, as masas dos elementos que forman un mesmo composto atópanse sempre en proporción constante -Lei das proporcións definidas-
mA/mB = Cte
As reaccións químicas non se producen instantaneamente, tardan determinado tempo en producirse. Ás veces convén aumentar a velocidade e outras diminuíla. A magnitude velocidade de reacción mide arapidez coa que se produce unha reacción e defínese como o cambio de concentración dun reactivo ou producto co tempo (ΔC/Δt). Nós podemos intervir nas condicións para modificar a velocidade. Os factores nos que podemos influír son: concentracións, presión, temperatura e catalizadores, a influencia dos cales xustifícase mediante a teoría cinética de reacción química.
As disolucións son mesturas homoxéneas de dous ou máis compoñentes. Ao compoñente con maior proporción chamámoslle disolvente e aos outros solutos. As disolución tamén se preparan no laboratorio co obxectivo de que o contacto entre os reactivos sexa máis eficaz e a reacción se produza máis facil e rapidamente.
A diferencia dos compostos (sustancias) as disolucións NON teñen fórmula porque os compoñentes poden mesturarse en calquera proporción (lembremos que nos compostos a proporción de combinación entre os elementos é fixa e constante) e para caracterizalas utilizaremos o concepto de concentración. A concentración expresa a proporción de soluto na disolución e podemos dala de diferentes maneiras:
En todas as reaccións hai intercambios de enerxía que poden ser en forma de calor e/ou traballo. Centrándonos na calor, podemos clasificalas en dous grupos: a) exotérmicas, que dan calor ao ambiente e b) endotérmicas, que collen calor do ambiente. Hai algunhas reaccións que se empregan exclusivamente como fontes de calor (combustibles).
Aproximadamente, 90% dos 18 millóns de compostos coñecidos son de tipo orgánico. A auga representa do 60 ao 90% da materia viva, sen embargo, menos do 4% da porcentaxe restante (entre o 10 e o 40%) é anorgánica; a porcentaxe restante é orgánica. A bioquímica é a parte da química que estudia a materia viva e baséase na química orgánica. As roupas, as casas, os mobles, os combustibles, as mediciñas, os productos de belleza, os abonos, etc. son principalmente productos de tipo orgánico.
Todos os compostos orgánicos conteñen un elemento básico e común que é o carbono. Chámanse compostos orgánicos porque nos comezos da química pensábase que procedían unicamente de organismos vivos (animais e plantas), ata que no 1828 o químico Wöhler fabricou urea (composto orgánico) a partir de cianato de amonio (composto anorgánico). Estes compostos estan formados pola combinación de relativamente poucos elementos: C, H, O, N, P, S, Cl, Br, e poucos máis e enlazados entre si mediante enlaces covalentes. Agran cantidade de compostos orgánicos coñecidos está baseada na capacidade -única entre os elementos do SP- do carbono de enlazarse consigo mesmo formando cadeas e aneis que son completadas polos outros elementos da lista anterior.
O petróleo é unha mestura de sustancias orgánicas moi importante na civilización actual, pois é unha das fontes de combustibles fósiles (hidrocarburos) e tamén de productos orgánicos básicos que se empregan na fabricación de todo tipo de obxectos industriais (adhesivos, analxésicos, anticonxelantes, plásticos, fibras textiles, etc.). A combustión dos hidrocarburos produce como productos CO2 e H2O que son gases de efecto invernadoiro. O desmesurado consumo deste tipo de combustibles está a provocar un aumento considerable deste efecto o cal ten xa consecuencias comprobadas de alarmantes efectos.
Outro problema derivado da producción industrial de plásticos, envases e embalaxes consiste na sua gran estabilidade química -na pouca reactividade química- e longa vida, o cal vai a plantexar problemas de reciclaxe destes materiais ... son todos reclables? pódense reutilizar? como?.
Anterior: ENERXÍA