| ESTUDIO DA COMBUSTIÓN DO CACAHUETE USANDO DISTINTOS MODELOS DE CALORÍMETRO | |
|
As reaccións de combustión son combinacións dunha substancia, chamada combustible, co osíxeno que se descompón noutras máis simples liberando enerxía. Se o combustible contén carbono un dos productos da reacción é o dióxido de carbono (CO2). Este tipo de reaccións se dan, por exemplo, cando algo se queima. Se queimamos un cacahuete a reacción acontece segundo a seguite ecuación química: |
|
|
Nas mitocondrias das células se producen reaccións de combustión que utilizan como combustible os nutrintes. A enerxía liberada nesta reacción, chamada respiración celular, se utiliza para realizar as funcións vitais das células (movemento, crecemento, transporte de substancias entre as células e o exterior, reproducción, etc). Anque globalmente a reacción química é a mesma ca representada arriba, a respiración celular faise en moitas etapas para aproveitar mellor a enerxía que se libera. A cantidade de enerxía que produce un alimento chámase valor enerxético dun alimento e é a mesma que se libera cando se queima e pode ser medida cun calorímetro. Os calorímetros miden a enerxía liberada nunha reacción química xa que esta se aproveita para quentar auga. Medindo o aumento de temperatura dunha cantidade coñecida de auga se pode calcular a enerxía liberada. O problema está en que parte da enerxía produccida na reacción se perde, para o cal probamos con distintos sistemas de aillamento que aparecen nas fotografías. A eficacia do calorímetro se refire a porcentaxe da enerxía que se aproveita para quentar a auga e consideramos o 100 % como o valor enerxético do cacahuete que ven na etiqueta da bolsa (626 kcal/100g) |
|
| Valor obtido: 217
kcal/100g
Eficacia do calorímetro: 34,7 % |
|
| Valor obtido: 209
kcal/100g
Eficacia do calorímetro: 33,3 % |
|
| Valor obtido: 240
kcal/100g
Eficacia do calorímetro: 38,3 % |
|
| Valor obtido: 207
kcal/100g
Eficacia do calorímetro: 33,1 % |
|
|
AUTORES/AS: Juan Alonso, Samuel Ballesteros, Mónica Collazo, Daniel García, Felipe Graña, David Leirós, Alberto Núñez, Ana Belén Salgado. DIVER-3 ÁMBITO CIENTÍFICO |
|
|
CONCLUSIÓNS Como se pode ver polos datos os nosos calorímetros non son moi eficaces e so aproveitan aproximadamente a terceira parte da enerxía liberada na combustión. Os calorímetros que utilizan botellas de refrescos (PET) como elemento aillante son os menos eficaces, non existindo diferencias significativas co calorímetro que non ten aillamento. O calorímetro que utiliza latas de refresco (aluminio) como aillante parece ser algo máis eficaz, probablemente debido ó tipo de material. |
|
|
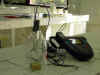
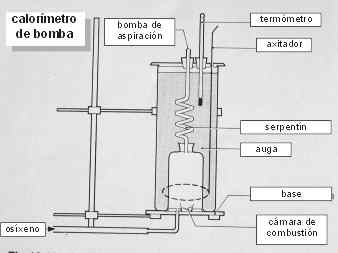
O CALORÍMETRO DE BOMBA Para solventar estes problemas nos laboratorios utilízanse os calorímetros de bomba, do que aquí tes unha foto e un esquema. |
|
|
|
|