volver ao índice de fichas
cinética
- A velocidade dunha reacción química mide como cambia a concentración
dun producto (ou reactivo) co tempo. A ecuación da velocidade proporciona
a relación entre a velocidade da reacción e a concentración. Esta
ecuación inclue unha constante de velocidade, k, e concentracións
elevadas a un expoñente que indica a orden da reacción con respecto a esa
especie química. A orden da reacción determínase medindo como cambia a
velocidade da reacción cando a concentreción inicial da especie cambia,
P.ex aA+bB → Productos.
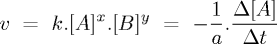
- Para que se produza unha reacción química é necesaria unha enerxía
mínima (para que as colisións entre as partículas reaccionantes sexan
mínimamente eficaces), chamada enerxía de activación, Ea. As
reacción rápidas teñen Ea pequenas e as lentas Ea
grandes. Os catalizadores cambian a rapidez coa que se producen as
reacción (posibilitando un camiño alternativo ao directo) facendo
diminuir (aumentar, segundo conveña) a Ea.
- Cando a T aumenta hai máis moléculas cunha E maior ca
Ea e por iso a velocidade da reacción aumenta coa
temperatura.
- Cando a C aumenta hai máis moléculas por unidade de volume e
por iso tamén aumenta a probabilidade de choque entre as partículas
reaccionantes e loxicamnete o efecto consistirá en aumentar a rapidez da
reacción.
Anterior: TERMODINÀMICA ;
Seguinte: EQUILIBRIOS
Last modified: Tue Jun 8 23:02:31 CEST 2004