O electrón xira nuha órbita circular e tendo en conta o primer postulado de Bohr, temos
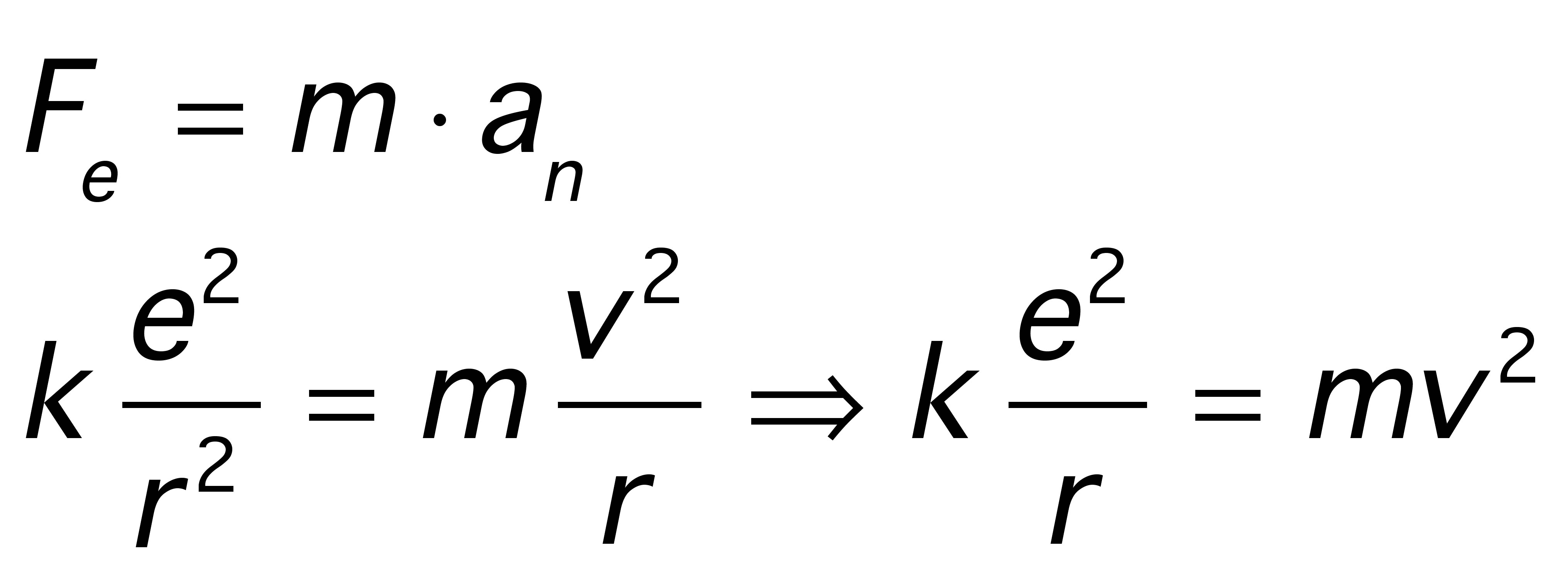
despexamos v da expresión do momento angular
![]()
e a sustituimos na expresión de arriba
![]()
despexando r temos a expresión do radio
![]()
sustituindo os valores das constantes obtemos o valor do radio dando valores a n
![]()
A enerxía total do electrón é a suma da enerxía cinética e a enerxía potencial
![]()
como
![]()
A enerxía total do electrón é
![]()
sustituindo os valores das constantes obtemos o valor da enerxía que depende do valor de n.
![]()
Ao número n se denomina número cuántico principal, e indica o nivel enerxetico que ten o electrón